Composition de l’air – Cours – 4ème – Physique – Chimie – Collège
- Quelles sont les proportions des deux principaux gaz constituant l’air ?
- Quel est le gaz nécessaire à la respiration ?
- Quelle est la différence entre un gaz et une fumée ?
- Méthode : identifier le dioxygène
I. Qu’est-ce qu’une atmosphère ?
Une atmosphère: c’est une couche gazeuse qui entoure un astre.
Exemples d’astres qui ont une atmosphère: la Terre, Mars, Venus, Jupiter, le Soleil, Titans.
Exemples d’astres dépourvus d’atmosphère: la Lune, mercure, pluton.
Remarque: La présence d’une atmosphère autour d’un astre ne garantit pas que celle-ci puisse abriter la
Vie.
1. Caractéristiques et couches de l’atmosphère terrestre.
L’atmosphère terrestre correspond à la couche d’air qui entoure la Terre.
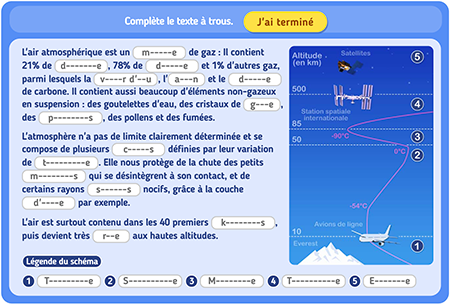
On estime qu’elle a une épaisseur d’environ 500 km. Les variations de température dans l’atmosphère terrestre ne sont pas régulières. Dans certaines zones elle diminue et dans d’autres elle augmente ce qui a conduit distinguer plusieurs couches:
La troposphère de 0 à (en moyenne) 12 km d’altitude. La température y diminue avec l’altitude. C’est dans cette couche que se déroulent les principaux phénomènes météorologiques. La troposphère concentre 90% de l’air contenue dans l’atmosphère.
La stratosphère s’étend en moyenne de 12 à 50 km d’altitude. La température y augmente régulièrement.
La mésosphère s’étend en moyenne de 50 à 80 km d’altitude. La température y augmente régulièrement.
La thermosphère qui s’étend en moyenne de 80 à 500 km
Remarque: on inclut également parfois une couche supplémentaire appelée exosphère qui permet la transition vers le vide interplanétaire mais qui est encore protégée des particules émises par le Soleil grâce au champ magnétique terrestre.
II. La composition de l’air
L’air est un mélange de nombreux gaz mais ses deux principaux constituants sont:
le dioxygène (21%)
le diazote (78%)
Remarque: le dioxygène est souvent appelé simplement oxygène dans la vie courante mais ce terme n’est chimiquement pas exacte (l’explication sera donnée lors de l’étude des constituants microscopiques de la matière)
Il reste également de 1% d’autres gaz: argon, néon, dioxyde de carbone, ozone etc. Cette composition n’était pas la même lorsque la Terre s’est formée et elle a été modifiée profondément par l’apparition de la vie: Les algues bleues, aussi appelées cyanobactéries furent les première formes de vie à produire du dioxygène il y 3,8 milliards d’années.
III. L’air et la vie :
L’étude de la respiration humaine (et animale) permet de montrer que par rapport à l’air inspiré (qui pénètre dans les poumons) l’air expiré (rejeté par les poumons):
- Contient moins de dioxygène.
- Contient autant de diazote.
- Contient plus de dioxyde de carbone.
Cette comparaison de l’air inspiré et de l’air expiré permet de déduire que la respiration:
- Produit du dioxyde de carbone.
- Consomme du dioxygène.
- Ne nécessite pas de diazote.
Le dioxygène est donc nécessaire à la vie.
Remarque: Les proportions de dioxygène et de dioxyde de carbone dans l’air restent stables car le jour les plantes consomment du dioxyde de carbone et produisent du dioxygène.
Ce phénomène appelé photosynthèse conduit à un équilibre et maintien des proportions stables de dioxygène et de dioxyde de carbone.
III. Quelle est la différence entre un gaz et une fumée :
Etude d’un document : observation de cette expérience, on fera traverser de l’air à travers un filtre propre, après sur un autre filtre de même caractéristiques on fera traverser de la fumée.
Observation :
Lorsque l’air traverse seul le filtre, le filtre reste blanc
Lorsque la fumée traverse le filtre, le filtre se noircit.
Interprétation :
Les molécules qui constituent les gaz de l’air passent facilement à travers un filtre, alors que les particules qui constituent les fumées sont solides et suffisamment grandes pour être arrêtées par le filtre.
Conclusion : Une fumée contient des particules solides en suspension de taille supérieure aux molécules qui constituent les gaz de l’air.
III. Test de reconnaissance du dioxygène :
Expérience : On réalise l’expérience schématisée ci-dessous, pour reconnaître le dioxygène il faut
- Enflammer la bûchette (Prudence : cheveux longs)
- Souffler la flamme pour laisser un point incandescent
- Pencher le tube à essais
- Ouvrir le tube à essais
- Introduire la bûchette.
Schéma et observations du test :
Préparation du dioxygène par réaction chimique
On produit du dioxygène en faible quantité à partir d’une réaction chimique : on fait agir de l’eau oxygénée sur une solution de permanganate de potassium :
Comment s’assurer que le gaz produit dans l’expérience précédente et le dioxyde ??
On place dans le tube à essais une bûchette présentant un point incandescent. Elle s’enflamme en présence de dioxygène.
Le gaz obtenu par réaction chimique a les mêmes propriétés que le dioxygène prélevé dans la bouteille. Le dioxygène obtenu par réaction chimique est identique à celui présent dans l’air.
Composition de l’air – Cours – 4ème – Physique – Chimie – Collège rtf
Composition de l’air – Cours – 4ème – Physique – Chimie – Collège pdf